【元素分析】有機構造決定(1)
<この記事の内容>:高校化学、有機分野の構造決定問題の解法・手順を紹介していくシリーズ第1弾!
今回は元素分析の方法(実験装置それぞれの意味や、よく問われる乾燥剤・酸化剤の意味など)から、組成式・さらに分子式の決定に必要な計算問題までに詳しく解説します。
目次(タップした所へ飛びます)
元素分析:有機構造決定の手順
全体的な考え方をまずまとめています。具体的な解法を読みたい方は、元素分析のところまでスクロールしてください。
構造決定問題への心構えと解き方の流れ(総論)
構造決定の問題はいわば高校における有機化学の集大成であり、また理論化学や無機化学とも融合しパズルを解いて行くような特有の難しさがある範囲です。
それ故に苦手意識がある人が多いですが、苦手な人ほど「行き当たりばったり」に構造決定を解いている事が多いです。
しかし実際はかなり論理的で、方法もほとんど決まっています。
ですから、実戦では「パズル」ではなく、一定のメソッドの下で、問題文をよく「読解」し、自分の知識と照らし合わせて解いて行く事になります。
知識と言ってもなるべく苦労せず自然と覚えて行くように書いていくので、ぜひついて来てください。
元素分析とは
では、構造決定のはじめに行う組成式の調べ方について見ていきます。(参考:「組成式と分子式の違い」については左の記事で詳しく扱っています。)
装置と仕組み:組成式の調べ方
この組成式を調べる実験と、それぞれの実験器具や化学物質は「意味」を問われることが多いので、しっかりと仕組みを理解しておく必要があります。
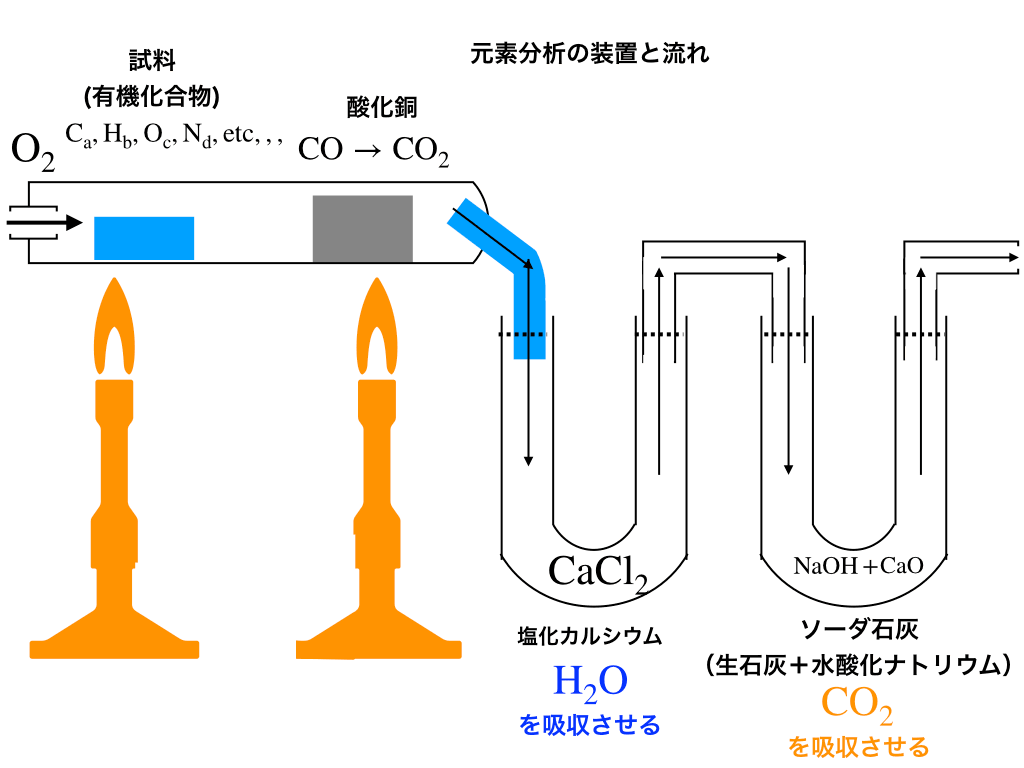
【組成式を調べる装置・手順】
元素分析の手順1:酸素を入れて試料を燃焼させる
今組成式を調べる対象である「試料」には、炭素や酸素、水素、窒素、などなど様々な元素が混じっています。
はじめにこれらを燃焼させる事で、水素は\(\mathrm{H_{2}O}\)、炭素は\(\mathrm{CO}_{2}\)などに変化します。
この「水」や「二酸化炭素」を、後で紹介する乾燥剤で吸収して「試料」がどのようなものか分析します。
酸化銅の役割とは
試料が全て燃焼しないと正確な組成式を調べることができないので、【酸化剤】の役割を果たす酸化銅を設置する事で、完全燃焼させます。
すなわち、\(\mathrm{CuO+CO}\rightarrow \mathrm{CO_{2}+Cu}\)となることで一酸化炭素を二酸化炭素へと変化させているのです。(参考:「酸化剤と還元剤を解説」)
乾燥剤の順序:塩化カルシウムが先な理由
乾燥剤には以下の塩化カルシウムとソーダ石灰を用います。
順序を逆にすると、その時点で正確な分析が不可能になってしまうので、その理由とともに注意して覚えましょう。
\(\mathrm{CaCl}_{2}\)→水素を吸収
まず先に塩化カルシウムに通して、\(\mathrm{H_{2}O}\)を吸収させます。ここでの質量の増加分から試料の水素の量を調べます。
ソーダ石灰→塩基性→炭素を吸収
「ソーダ石灰」という化合物があるわけではなく、NaOH(水酸化ナトリウム)とCaO(生石灰:酸化カルシウム)の混合物のことを指すので要注意です。
そして、NaOHが含まれている(強塩基)からも分かる通り、ソーダ石灰は\(\mathrm{CO}_{2}\)を吸収します。
(二酸化炭素は水に溶けると炭酸になる→塩基と反応する)
ここで、\(\mathrm{CO}_{2}\)を吸収させて試料中の炭素”C"の量を調べます。
このソーダ石灰は\(\mathrm{H}_{2}\mathrm{O}\)も吸収してしまう為、必ず塩化カルシウムの後に設置します。
\(\mathrm{H}_{2}\mathrm{O}\) \(\mathrm{CO}_{2}\)
\(\mathrm{CaCl}_{2} \) : ◯ ×
ソーダ石灰 : ◯ ◯
酸素のはかりかた
試料となる有機化合物が炭素・酸素・水素だけからなる場合は、もともとの
{試料の質量}ー{(炭素+水素)の質量}を計算することで求めることができます。(逆に言えば、試料を燃焼させる際に外部から酸素を供給しているため、もともと試料にあった酸素はこの方法でしか計算できません。)
その他の元素
問題文中のヒントや、「炎色反応」などからその他の元素を調べます。
比を使って組成式を求める
\(\mathrm{C_{x}H_{y}O_{z}}\)
複雑になってくると、\(\mathrm{C_{\alpha}H_{\beta}O_{\gamma}N_{\delta}}\cdots\)と続いていきますが、初めのうちはこの三つの元素からスタートします。
例題と解説
例題1:炭素、酸素、水素の三つの元素からなる73(mg)の化合物Aを<図1>で示した装置で完全燃焼させた。
この時、塩化カルシウムを含む乾燥剤の重量が81(mg)、ソーダ石灰を含む乾燥剤の重量は176(mg)増加した。
この時の化合物Aの組成式(実験式)をもとめよ。
まず塩化カルシウムの質量は”水”を吸収して81(mg)になっています。
そこで、その\(\mathrm{H_{2}O}\)中の水素の量を求めるために、水の分子量(18)分の水素2つ分の式量(2)を計算し、これをHの原子量で割る事で水素のmol数が求まります。
(単位がmgなので、計算の際に\(10^{-3}\)をつけて単位をgに合わせています。)
$$81\times10^{-3}\times \frac{2}{18}\div 1=9\times 10^{-3}$$
次に、ソーダ石灰が二酸化炭素(分子量44)を吸収(そのうち12が炭素)→炭素の量(mol)が分かるので、
$$176\times 10^{-3}\times\frac{12}{44}\div 12=4\times 10^{-3}$$
残りは酸素のはずなので、
73-(9+48)=16(mg)
\(16\times 10^{-3}÷16=1\times 10^{-3}\)
これで、C,H,Oそれぞれの比が計算できます。(ここでは全てに\(10^{-3}\)がついているので、打ち消すことができ、結果=炭素:水素:酸素=4:9:1
(∴)組成式\(\mathrm{C_{4}H_{9}O}\)
組成式から分子式へ
組成式を求めおわると、次に分子式を確定させる作業に入ります。
分子量を計算:その方法
なぜなら、組成式はあくまでも原子の比なので、同じ組成式で違う化合物というものは無数にあり得ます。
そこで、分子式に直してあげる必要があります。
この時に『分子量』を求める(問題で与えられていればそれを使います)必要があり、その方法として
・「浸透圧の求め方とファントホッフの式」<<で紹介している『浸透圧』を利用する
・「凝固点降下・沸点上昇度」<<を利用する
・「理想気体の状態方程式”PV=nRT”」のnをMとwで表したバージョン:\(PV=\frac{w}{M}RT\)を式変形して利用する。
などの方法を使用します。
分子式の決定
ここでは、先ほどの例題と解説1での組成式を分子式に直す作業を実際にやってみます。
例題1-2:さらに、この有機化合物Aの分子量が146であることがわかっている時、Aの分子式を表せ。
Aの組成式は\(\mathrm{C_{4}H_{9}O}\)ですが、これは『最も簡単な整数比』なので実際にはnを使って\(\mathrm{(C_{4}H_{9}O)_{n}}\)と表すことができます。
分子量は\((12×4+9×1+16×1)_{n}=73n\)。
ここでAの分子量:146より
146=73nなので、n=2
(∴)各元素の比をそれぞれ2倍する事で次のように有機化合物Aの分子式が求まります。
\(\mathrm{C_{8}H_{18}O_{2}}\)・・・(答)
有機構造決定シリーズ記事一覧とまとめ
・元素分析の実験装置について、名前はもちろん順番やその理由まできっちりと理解して記憶しておく事。
・実験から引き算・比の考え方を用いて組成式を求め
↓
・分子量から分子式を決定する流れ
を理解し、できれば問題集の簡単なものでも解いて慣れていきましょう。
次回:不飽和度〜異性体
次回は、今回の手順で求めた分子式や、その発展問題を『不飽和度』という値を求めることによって、さらに構造決定を進める方法を紹介します。
有機構造決定1:「(今ここです)」
その二:「不飽和度の意味と計算公式を解説」
その三:「各種異性体の意味と書き出しの方法」
〜〜 〜〜
有機その一:「有機化学の全体像(意味・分類)の総整理」
有機その二:「脂肪族鎖式化合物のまとめ(1)」
有機その三:「(作成中です)”ベンゼン環”と芳香族化合物」
今回も最後までご覧いただきまして、有難うございました。

