
有機構造決定:(3)
色々な異性体とその書き出し(数え方+書き方)
<この記事の内容>:これまでこのシリーズでは、「元素分析の仕方・分子式の決定とその例題」、「不飽和度の意味と構造決定への利用法」を紹介してきました。
今回はそれらの知識をもとに『異性体』についてわかりやすく解説していきます。
目次(タップした所へ飛びます)
異性体とは?
異性体とは同じ化学式ではあるが、形が違うもの、例えば\(\mathrm{CH_{3}-O-C_{2}H_{5}}\)と\(\mathrm{CH_{3}-CH_{3}-CH-OH}\) などのことを言います。
もう少し詳しく異性体の種類について解説します。
構造異性体とは
「化学式の種類まとめと例」で紹介した「構造式が異なる」が「分子式は同じ」物を構造異性体と呼びます。
主に3パターンがあり、以下でそれぞれ解説していきます。
構造異性体:炭素骨格が違うタイプ
有機化合物を構成する、いわば『骨組み』となるC原子が4つを超えると、枝分かれや真っ直ぐな鎖状の異性体が生じます。
\(\mathrm{CH_{3}-CH_{2}-CH_{2}-CH_{3}}\)と、\(\mathrm{CH_{3}-CH\underbrace{(CH_{3})}_{ここで枝分かれ}-CH_{3}}\)
他にも、二重結合・三重結合を含む化合物の場合、その結合がどこにあるかによって別々の異性体とみなします。
構造異性体:官能基の種類が違うタイプ
2番目:例えば、アルコールとエーテル、アルデヒドとケトンのように分子式が同じであるが、示性式で表すと異なる(当然性質も違うものとなります)タイプです。
\(\mathrm{CH_{3}-CO-CH_{3}}と\mathrm{C_{2}H_{5}CHO}\)
構造異性体:官能基の接続位置が違うタイプ
ヒドロキシ基が右端or左端についている場合と真ん中についている場合でも構造異性体となります。
\(\mathrm{CH_{3}-CH\underbrace{(OH)}_{ここで枝分かれ}-CH_{3}}\)
\(\mathrm{CH_{3}-CH_{2}-OH}\)
ここまで例示してきた有機化合物は、炭素数も少なく比較的楽に見分けられますが、もう少し大きい分子になると、この構造異性体だけで何パターンもの可能性が出て来ます。
立体異性体
構造異性体だけでも大概ややこしいのですが、さらに注意して書き出す必要があるのはこの『立体』異性体です。
幾何(シスートランス)異性体
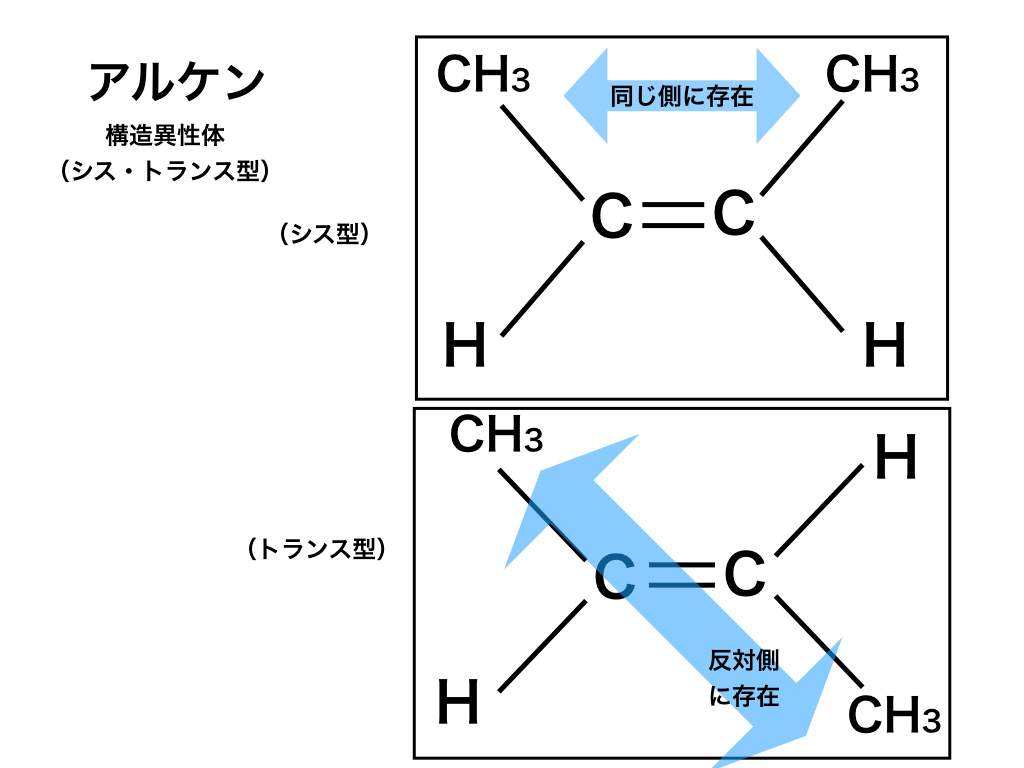
化合物中にC=Cの炭素間二重結合があると、以下のアルケンの図のように2つの異性体が存在します。
これは、二重結合によって自由に回転ができず平面上に張り付いたような状況が起こるためです。
(上のシス型のC=C部分を”もし180度”回転させられれば下のトランス型と同じになりますが、それができないということです。)「脂肪族”鎖状”炭化水素の分類を分かりやすく!」
光学異性体(鏡像異性体)
もう一つの立体異性体が『光学(鏡像)異性体』というものです。
鏡像異性体と言われる理由は、異性体同士が鏡でうつしたように”どう動かしても決して同じ形にならない”ためです。
なぜ『光学』という名前がついているかについてもう少し詳しく紹介しておきます。
同一の化学式で表される、”光学異性体D、と、L”があったとすると、旋光性という、D型に光波を入れると右回転し、L型に入れると左に回転して出てくる性質を持つからです。
この違いによって、一方はうま味として感じられるが・もう一方にはその様な味がない(グルタミン酸)など違う性質を持つこともあります。
不斉炭素原子とは
さらに、光学異性体を考える際に欠かせないのが『不斉炭素原子』と呼ばれ、一般に\(\mathrm{C}^{\ast}\)で表される”ちょっと特別な”炭素が存在することです。
不斉炭素原子は、その4本の手が一つずつ全て違う官能基や原子(原子団)、分子と結合しているものの事です。
注意すべきところは、一見同じメチル基(\(\mathrm{-CH_{2}}\))と結合しているように見えても、その先の構造が異なるような場合、別のものとして考える点です。
最も基本的な乳酸
この不斉炭素原子を持つ最も単純(基本的)な化合物が乳酸です。
\(\mathrm{HO-C^{\ast}\underbrace{(CH_{3})}_{ここで下に枝分かれ}\overbrace{H}_{ここで上に枝分かれ}-COOH}\)
アミノ酸と鏡像異性体
アミノ酸(Gyを除く)もまた、光学(鏡像)異性体です。
グリシンだけは、炭素原子:Cの四つの手がHが2つとアミノ基に一つ、カルボキシル基に一つ伸びているため不斉炭素原子とならないためです。
逆にそれ以外のアミノ酸は全て鏡像異性体であると言えます。
アラニン:不斉炭素原子の周りにカルボキシル基、アミノ基、H原子、メチル基(CH_{3})がそれぞれ結合している、アミノ酸の中で2番目に簡単な構造をしています。
\(\mathrm{H-C^{\ast}\underbrace{(CH_{3})}_{ここで下に枝分かれ}\overbrace{NH_{2}}_{ここで上に枝分かれ}-CH_{3}}\)
(詳しいアミノ酸の解説は、「アミノ酸(天然高分子シリーズ)」を作成中です。)
異性体書き出しのコツ・チェック項目
・不飽和度から、二重・三重結合の数と位置で場合分け
・一見構造異性体に見えても、C骨格が実は同じ(特に枝分かれがある異性体)場合をチェック
・官能基の位置と(アルデヒド・ケトン)、などの組に注意
異性体の書き出し・種類の数を求める問題
ここまで、異性体の基礎知識を解説してきました。
ここからは、実際に分子式から異性体を書き出して、その種類を数えてみましょう。
例題
次の分子式で表される化合物の異性体を全て書き出し、その種類の数を答えよ。(問題を追加していきます。2020/03/20)
(1):\(\mathrm{C_{4}H_{10}O}\)
(手元にある紙に、構造:幾何:光学異性体に気を付けて実際に書き出して見てください。)
解説と異性体の構造式
では解説と、異性体の数、構造を答えあわせしていきましょう。
(1):
step1:まずは何よりも先に不飽和度のcheckです。
$$I=\frac{4\times 2+2 -10}{2}=0$$
よって、全て単結合でできていることがわかります。
step2:次に、「どのような炭素骨格があり得るか」を考えます。
すると以下の解説図のように、一直線上orT字形の2パターンに大きく分けることが可能です。
step3:step2で書き出した2パターンのC骨格に、酸素原子を入れる場所(=官能基ーOH、ーOー、を付ける・入れるところ)を慎重に考慮すると、、、
(下の図ではヒドロキシ基以外の水素原子は省略しています。)
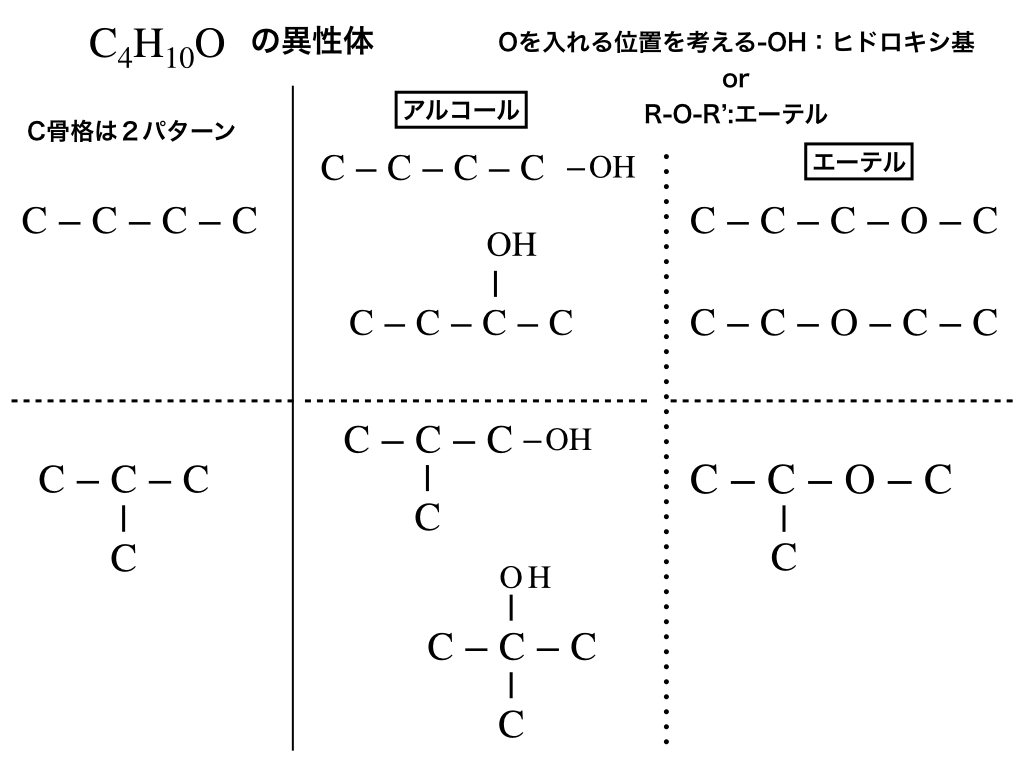
結果:7種類・・・(答)となります、
異性体まとめと次回へ
有機の構造決定(大抵の大学入試の化学で出題され、25%くらいの点数を占めることが多いです。)の問題では、異性体を書き漏らした(もしくは同じものをダブルで数えてしまった)時点で、その大問は0点です。
よって、もれなく+重複なく全ての異性体を書き出す訓練が必要になります。
大抵の問題集に異性体の問題が載っているので、そこでミスしなくなるまで繰り返し(数をこなして)解いておいて下さい。
この段階では難しい有機専門の問題集でなくとも、一般的な化学の問題集で構いません。
(参考:「演習にオススメな化学の参考書」)
何よりも確実に漏れなく書き出せることが重要です!
次回は問題文中に書かれている、構造決定のヒントになる“フレーズ”などをまとめていきます。
有機構造決定の記事一覧
シリーズ1:「元素分析と分子式の決定」
シリーズ2:「不飽和度の意味と計算方法」
シリーズ3:「(今ココです)」
シリーズ4:「(作成中です):構造決定を助けるhintsまとめ」
最後までご覧いただきまして、有難うございました。
【受験・総合学習メディア】:「スマナビング!」では、読者の皆様からのご感想を募集しています。ぜひコメント欄にお寄せください。
(※:個々の問題・証明の質問等、全てにお返事ができない場合があります。ご了承ください)
・その他の「お問い合わせ/ご依頼/タイアップ」等に付きましては、【運営元について】ページよりご連絡下さい。

