目次(タップした所へ飛びます)
今回は有機化学の根幹である炭素と炭素の結合について詳しく説明していきます。
今日の内容は一部の進学校と、上位レベルの予備校/クラスでしか扱われていません。
しかし、難しい内容ではない上、理屈で有機反応が分かる様になるので、本来理系ならば皆知っておくべき事なのです!是非読んでみてください。
*この記事では大学受験を有利に進める為に感覚的な理解を優先して記述しています。更に厳密な理論は是非大学で学んで下さい*
※記事の改良と有機反応の理解が進むように新設した人気の記事との連携を追加しました。まだ読んでいない方は是非この記事とリンク記事を読んで下さい!(18’2/19更新)
さてCーC結合には、「単結合・二重結合・三重結合の3つがある」と普通、学校では教えられています。
しかし、それではベンゼン環の様な例外が出て来た時などに1.5重結合!?などと曖昧にされてしまいます。
ベンゼン環の理解が曖昧だとベンゼン環を中心とする芳香族の反応が只の暗記になってしまい苦痛でしかないです。
では本当の炭素間結合はどういう物なのでしょうか?ココでも電子が重要な役割を担う事になります。
炭素間結合は大きく2つに分けることができます。(実際はδデルタ結合やφファイ結合等々有りますが、大学受験レベルでは2つで十分です)
一つはσ結合(シグマ結合)
もう一つはπ結合(パイ結合)です。
シグマ結合とは?
σ結合とは、簡単に言うと単結合の事で、互いの不対電子を共有して強く結びついている状態です。
パイ結合とは?
π結合とは、二重結合/三重結合の内、σ結合でない方。
三重結合であればσ結合でない残り2つの結合で、こちらは図の様にもやっと雲のように上下で弱く結ばれているものです。
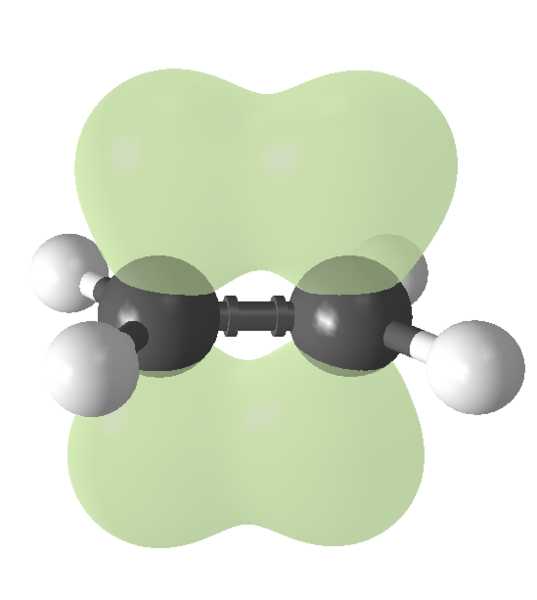
図からもσ結合がシッカリ、π結合がよわ〜く結びついているのがわかるかと思います。
アルキン、アルケンはこの弱いπ結合が1つor2つあるおかげで、簡単に結合が切れて、反応しやすいのです。(臭素付加など)
一方でアルカンやそれに(-OH)基が付いたアルコールはσ結合だけなので、これを反応させる(=結合を切る=共有電子対をバラバラにする)為には強い酸化剤等が必要になってくるのです。
(例:エタノールは過マンガン酸カリウムと言う強力な酸化剤で酢酸へと変化します。)
そして本題のベンゼンです。
ベンゼン環は1.5重結合や、単結合と二重結合が入れ替わっているのではありません!
ではどういう状態なのか?
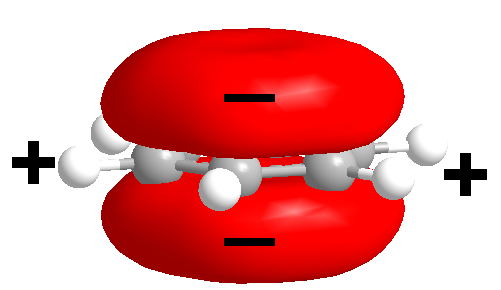
それは炭素が六角形をσ結合で作り、その上下で残りの電子がπ結合で結びつき、ドーナッツの様な雲状の電子雲にサンドイッチされた様な形をしています。
image by File:Benzene Quadrupole.png -Wikipedia
Author :Michael.hell at English Wikipedia
これを「共鳴」や「非局在化」していると言うのですが、重要な事は「電子雲は電子で出来ているので、当然負の電荷を持っている」という言う事です。
ベンゼン環は上下にマイナスの電荷を持つ電子雲に挟まれています。
大切な事なので二度言いました!
何故大切なのでしょう?
例えばベンゼンからフェノールを作る方法は超頻出です。主に4つ製法がありますが、何故ベンゼン環に直接(-OH)ヒドロキシ基をくっ付けないのでしょう?
それはベンゼン環が負の電子雲をまとっているので(3回目です)、マイナスの電荷を持つヒドロキシ基と反発し合うからなのです。
だからわざわざ色々な製法が生み出されたのです。
※電子と有機化学反応について、まとめた記事(リンク)を執筆しました!未読の方は是非読んで下さい!
まもなく公開するフェノールの製法まとめ記事の理解がかなり違ってきます。(18‘2/19更新)
この様に少し大変ですが、本当の電子の振る舞いを考えると、有機化学は決して暗記分野などではなく、
全て意味がある事がわかると思います。
そして意味が理解出来た時、自然に有機反応は覚えている事でしょう。
今日は大変だったと思いますが、ここまで読んで下さって有難うございます!
次回はいよいよベンゼンからフェノールの製法を丸暗記でなく、納得しながら自然と覚える様に解説します。
続編完成しました!>>「フェノールの製法を徹底解説!ベンゼンの正体を知って楽々理解!」<<

